Khối lượng mol là gì? Công thức tính lượng mol?
Khối lượng mol (M) của một hóa học là lượng của 1 mol hóa học cơ, được xem bởi gam (g/mol). Nó có mức giá trị bởi tổng lượng vẹn toàn tử của những yếu tố vô phân tử hóa học cơ.
Khối lượng mol được xem theo đuổi công thức sau đây:
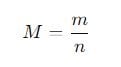
Trong đó:
- M: Khối lượng mol (g/mol)
- m: Khối lượng của hóa học (g)
- n: Số mol của hóa học (mol), tính theo đuổi công thức: n = m / M
Ví dụ:
Tính lượng mol của hóa học X, hiểu được 2 mol hóa học này còn có lượng là 50 gam.
Bước 1: Thay số vô công thức
m= 50g (khối lượng của hóa học X)
n= 2 mol (số mol của hóa học X)
Bước 2: Tính lượng mol của hóa học X
M = m/n = 50/2 = 25 (g/mol)
Như vậy, lượng mol của hóa học X là 25 g/mol.
Lưu ý: tin tức "Khối lượng mol là gì? Công thức tính lượng mol?" nêu bên trên chỉ mang tính chất hóa học tìm hiểu thêm.

Khối lượng mol là gì? Công thức tính lượng mol? Học sinh lớp 8 cần thiết đạt đòi hỏi gì khi tham gia học mol và tỉ khối của hóa học khí? (Hình kể từ Internet)
Học sinh lớp 8 cần thiết đạt đòi hỏi gì khi tham gia học mol và tỉ khối của hóa học khí?
Căn cứ vô Chương trình dạy dỗ phổ thông môn Khoa học tập ngẫu nhiên phát hành tất nhiên Thông tư 32/2018/TT-BGDĐT quy tấp tểnh đòi hỏi cần thiết đạt so với học viên lớp 8 khi tham gia học phản xạ hoá học tập như sau:
Biến thay đổi vật lí và chuyển đổi hoá học | - Nêu được định nghĩa sự chuyển đổi vật lí, chuyển đổi hoá học tập. - Phân biệt được sự chuyển đổi vật lí, chuyển đổi hoá học tập. Đưa rời khỏi được ví dụ về sự việc chuyển đổi vật lí và sự chuyển đổi hoá học tập. |
Phản ứng hoá học | - Tiến hành được một trong những thực nghiệm về sự việc chuyển đổi vật lí và chuyển đổi hoá học tập. - Nêu được định nghĩa phản xạ hoá học tập, hóa học đầu và thành phầm. - Nêu được sự bố trí không giống nhau của những vẹn toàn tử vô phân tử hóa học đầu và sản phẩm - Chỉ rời khỏi được một trong những tín hiệu chứng minh với phản xạ hoá học tập xẩy ra. |
Năng lượng trong những phản xạ hoá học | - Nêu được định nghĩa và thể hiện được ví dụ minh hoạ về phản xạ toả sức nóng, thu sức nóng. - Trình bày được những phần mềm phổ cập của phản xạ toả sức nóng (đốt cháy than thở, xăng, dầu). |
Định luật bảo toàn khối lượng | - Tiến hành được thực nghiệm nhằm hội chứng minh: Trong phản xạ hoá học tập, lượng được bảo toàn. - Phát biểu được tấp tểnh luật bảo toàn lượng. |
Phương trình hoá học | - Nêu được định nghĩa phương trình hoá học tập và quá trình lập phương trình hoá học tập. - Trình bày được ý nghĩa sâu sắc của phương trình hoá học tập. - Lập được sơ thiết bị phản xạ hoá học tập dạng văn bản và phương trình hoá học tập (dùng công thức hoá học) của một trong những phản xạ hoá học tập rõ ràng. |
Mol và tỉ khối của hóa học khí | - Nêu được định nghĩa về mol (nguyên tử, phân tử). - Tính được lượng mol (M); Chuyển thay đổi được thân thuộc số mol (n) và lượng (m) - Nêu được định nghĩa tỉ khối, ghi chép được công thức tính tỉ khối của hóa học khí. - So sánh được hóa học khí này nặng trĩu hoặc nhẹ nhõm rộng lớn hóa học khí không giống phụ thuộc công thức tính tỉ khối. - Nêu được định nghĩa thể tích mol của hóa học khí ở áp suất 1 bar và 25 chừng C. - Sử dụng được công thức n(mol) = V(L)/24.79(L/mol) nhằm quy đổi thân thuộc số mol và thể tích hóa học khí ở ĐK chuẩn: áp suất 1 bar ở 25 chừng C. |
Tính theo đuổi phương trình hoá học | - Tính được lượng hóa học vô phương trình chất hóa học theo đuổi số mol, lượng hoặc thể tích ở ĐK 1 bar và 25 chừng C. - Nêu được định nghĩa hiệu suất của phản xạ và tính được hiệu suất của một phản xạ phụ thuộc lượng thành phầm chiếm được theo đuổi lí thuyết và lượng thành phầm chiếm được theo đuổi thực tiễn. |
Nồng chừng dung dịch | - Nêu được hỗn hợp là lếu thích hợp lỏng như nhau của những hóa học tiếp tục tan vô nhau. - Nêu được khái niệm chừng tan của một hóa học nội địa, độ đậm đặc Xác Suất, độ đậm đặc mol. - Tính được chừng tan, độ đậm đặc phần trăm; độ đậm đặc mol theo đuổi công thức. - Tiến hành được thực nghiệm trộn một hỗn hợp theo đuổi một độ đậm đặc cho tới trước. |
Như vậy, đòi hỏi cần thiết đạt so với học viên lớp 8 khi tham gia học mol và tỉ khối của hóa học khí như sau:
- Nêu được định nghĩa về mol (nguyên tử, phân tử).
- Tính được lượng mol (M); Chuyển thay đổi được thân thuộc số mol (n) và lượng (m)
- Nêu được định nghĩa tỉ khối, ghi chép được công thức tính tỉ khối của hóa học khí.
- So sánh được hóa học khí này nặng trĩu hoặc nhẹ nhõm rộng lớn hóa học khí không giống phụ thuộc công thức tính tỉ khối.
- Nêu được định nghĩa thể tích mol của hóa học khí ở áp suất 1 bar và 25 chừng C.
- Sử dụng được công thức n(mol) = V(L)/24.79(L/mol) nhằm quy đổi thân thuộc số mol và thể tích hóa học khí ở ĐK chuẩn: áp suất 1 bar ở 25 chừng C.
Nhiệm vụ của học viên lớp 8 là gì?
Căn cứ theo đuổi Điều 35 Điều lệ phát hành tất nhiên Thông tư 32/2020/TT-BGDĐT quy tấp tểnh về trách nhiệm của học viên lớp 8 như sau:
(1) Thực hiện nay trách nhiệm tiếp thu kiến thức, tập luyện theo đuổi lịch trình, plan dạy dỗ ở trong nhà ngôi trường.
(2) Kính trọng phụ thân u, cán cỗ, nhà giáo, nhân viên cấp dưới ở trong nhà ngôi trường và những người dân rộng lớn tuổi; kết hợp, hỗ trợ cho nhau vô tiếp thu kiến thức, rèn luyện; tiến hành điều lệ, nội quy mái ấm trường; chấp hành pháp lý của Nhà nước.
(3) Rèn luyện thân thuộc thể, lưu giữ gìn lau chùi cá thể.
(4) Tham gia những hoạt động và sinh hoạt luyện thể của ngôi trường, của lớp học tập, của Đội Thiếu niên Tiền phong Xì Gòn, Đoàn Thanh niên Cộng sản Hồ Chí Minh; hỗ trợ mái ấm gia đình, nhập cuộc làm việc và hoạt động và sinh hoạt xã hội, hoạt động và sinh hoạt đảm bảo môi trường thiên nhiên, tiến hành trật tự động đáng tin cậy giao thông vận tải.
(5) Giữ gìn, đảm bảo gia sản ở trong nhà ngôi trường, điểm công cộng; thêm phần kiến tạo, đảm bảo và đẩy mạnh truyền thống lịch sử ở trong nhà ngôi trường.
